Hola mis queridos amigos de Steemit, quiero compartir con ustedes la segunda parte de mi trabajo de investigación, espero sea de su agrado. En el post anterior se mostraron las aplicaciones que tienen los aceites vegetales en la industria, así como también otro tipo de sustratos, en este post se hablara de la hidroformilación de aceites vegetales (AV).
METODOLOGÍA
Hidroformilación de Aceites Vegetales
Como se dijo anteriormente, una de las aplicaciones industriales de los aceites vegetales (AV) es la obtención de biocombustibles; muchos investigadores han estado trabajando en esa área. Así, por ejemplo, en 2012, Sánchez y Huerta [20] realizaron una investigación experimental con el fin de evaluar las características principales del biodiésel de aceite de semillas de higuerilla modificada genéticamente como una fuente alternativa para la producción de biocombustible. Inicialmente, se realizó la caracterización física y química de la materia prima y posteriormente, se obtuvo el biodiésel por medio de la reacción de transesterificación del aceite con metanol usando metóxido de sodio como catalizador. Se caracterizó el biodiésel obtenido evaluando sus características físicas tales como, la densidad, índice de refracción, viscosidad cinemática, humedad y materia volátil, punto de ignición, poder calorífico y sus propiedades químicas como los índices de peróxido, acidez y yodo, la corrosión a la lámina de cobre y el contenido de metales. En este caso se obtuvo un biocombustible que cumple con la mayoría de los lineamientos estipulados (Norma ASTM D6751) que puede ayudar a disminuir el impacto ambiental y la dependencia causados por los combustibles fósiles.
Anwar y Bangher [21] estudiaron el contenido de aceite de las semillas de Moringa oleifera extraído con hexano, obteniendo rendimientos entre 38 y 42% y se encontró que el aceite contiene altos niveles de ácido oleico (hasta 78,59%), seguido por palmítico, esteárico, behénico, y ácido araquídico en niveles de 7,00, 7,50, 5,99, y 4,21%, respectivamente.
En 2015, Fernandes y col. [22] reportaronn el uso de aceite de Moringa oleifera como fuentes potenciales para la producción de biodiésel y aditivos antioxidante. El éster metílico M. oleifera fue preparado por una reacción de dos etapas y exhibió propiedades fisicoquímicas que cumplen los límites máximos de la Norma Europea (EN) 14214, con énfasis en el período de alta inducción (IP) de 19,3 h mínimo. Los extractos etanólicos de hojas de M. oleifera fueron evaluados como aditivos para aumentar el valor IP de biodiésel. Los resultados indican que el 98% m/m del extracto etanólico aumentó los valores de IP de biodiésel de soja 3,8 a 10,3 h, usando el 100 μg/g de extracto, que muestra un mejor rendimiento que el antioxidante tert-butil-hidroquinona sintético. Estos resultados evidencian el uso prometedor de M. oleifera no sólo para la producción de biodiésel, sino también como una fuente de aditivos antioxidantes para biodiésel con estabilidad a baja oxidación.
Actualmente grupos de investigación especialistas en este tema, han tenido la intención de introducir grupos funcionales oxigenados en el doble enlace carbono-carbono de algunos materiales naturales, tales como aceites vegetales o grasas animales con la finalidad de obtener biodiesel, [23] debido a que constituyen una fuente renovable de energía, además de que a partir de ellos también pueden obtenerse productos de alto valor agregado, tales como plásticos de alta eficiencia, adhesivos, lubricantes, y materiales para recubrimiento. Los aceites vegetales consisten en ésteres triglicéridos con tres ácidos grasos dominantes, oleico, linoleico y linolénico que poseen dobles enlaces internos, los dos primeros son los mayoritarios; un ester triglicérido típico se muestra en la Figura 2.
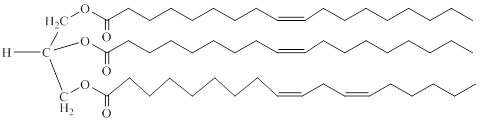
La hidroformilación homogénea, y más particularmente la bifásica acuosa, es un proceso ambientalmente amigable por el cual estos triglicéridos pueden ser convertidos en polialdehídos. Sin embargo, hasta la fecha este tipo de aplicaciones ha estado limitado desde el punto de vista de la catálisis homogénea y no ha sido reportado ningún ejemplo de catalizador bifásico acuoso.
Tal y como se mencionó anteriormente, Frankel y col. [9] reportaron el uso de complejos de cobalto para la hidroformilación [P(CO/H2) = 240-320 atm] de ésteres de ácidos grasos (OM y LM). Con el complejo Co2(CO)8, a 100-110ºC se obtuvieron los aldehídos como productos, mientras que a temperaturas entre 175 y 190 ºC se produjeron los alcoholes correspondientes; los compuestos obtenidos fueron mayoritariamente los del tipo ramificados (una mezcla de 5- hasta 13-formil- o hidroximetilestearato). Con el aumento de la temperatura y en presencia del catalizador modificado con tributilfosfina se incrementó la proporción del producto lineal (19-hidroxinonadecanoato de metilo).
Posteriormente, estos autores reportaron el uso de un sistema rodio/trifenilfosfina para la hidroformilación de AV y de derivados de ácidos grasos insaturados. La hidroformilación de OM fue realizada bajo condiciones moderadas de reacción (95-110 ºC y 30-130 atm CO/H2), obteniendo tanto el 9- y el 10-formilestearato de metilo (FEM) en un 90-99%. [11] Cuando el sustrato es un AV, a 100ºC y 70 atm de presión este sistema conlleva a una mezcla de FEM, formiloleato de metilo (FOM) y diformilestearato (DFE), mientras que a 150ºC y 100 atm los únicos productos fueron FEM y DFE. Los grupos de Frankel y Pryde han publicado revisiones de estos y otros trabajos relacionados con la hidroformilación de AV y moléculas modelo. [11,12]
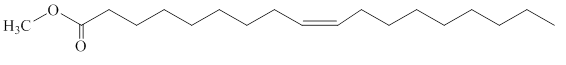
Frankel y Thomas [24], hidroformilaron grasas polinsaturadas utilizando un catalizador de rodio-trifenilfosfina. Posteriormente, van Leeuwen y col. [13] reportaron la hidroformilación de oleato de metilo (Figura 3) y de una mezcla de OM y LM en presencia de un catalizador de rodio modificado con el fosfito voluminoso tris(2-tert-butil-4-metillfenil)fosfito, obteniendo turnover numbers (TON) altos a 80-100 °C y 20 bar de gas de síntesis, usando tolueno como solvente. La hidroformilación de OM de alta pureza y grado técnico (conteniendo 84% de OM y 13,5% de LM) fue lograda obteniendo actividades bastante altas, las cuales fueron medidas como frecuencia catalítica (400-500 mol de producto por mol de catalizador por hora), bajo condiciones moderadas de reacción [T = 50-120ºC, P(CO/H2) = 50-80 atm en tolueno] para el OM puro y actividades un poco menores para el OM grado técnico.
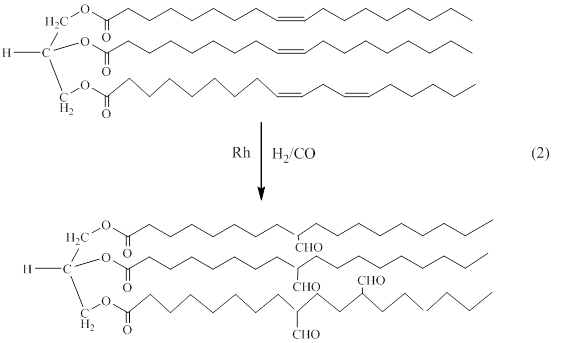
Kandanarachchi y col. [14, 15] reportaron la hidroformilación de aceites vegetales (aceite de soya) y moléculas modelo, utilizando catalizadores modificados de rodio con trifenilfosfina y trifenilfosfito (ec. 2).
Por todo lo anteriormente expuesto, en el presente trabajo se planteó realizar un estudio detallado de la hidroformilación homogénea y bifásica acuosa de OM y LM utilizando sistemas de rodio conteniendo ligandos fosfinas (mono-, bi- y tridentadas) y sistemas de cobalto, incluyendo un estudio cinético preliminar de la reacción de hidroformilación de OM y la hidroformilación de AV derivados de la moringa y de la borra de café con el catalizador más activo.
PARTE EXPERIMENTAL
Síntesis de Esteres Metílicos de Ácidos Grasos
El sustrato oleato de metilo se sintetizó por esterificación del ácido oleico con metanol en presencia de ácido sulfúrico como catalizador. En un balón de 250 mL se colocaron el ácido oleico (50 mL, 0,16 moles) y un exceso de metanol (12,7 ml, 0,31 moles), en presencia de ácido sulfúrico como catalizador (1,54 mL, 0,028 moles). La solución se colocó bajo reflujo constante con ayuda de una manta de calentamiento a una temperatura aproximada de 100 ºC, para así de esta forma eliminar la mayor cantidad de agua que se forma en la reacción. El pH de la mezcla (pH≈ 9) se reguló agregando bicarbonato de sodio. El líquido se separó por decantación y se lavó con éter dietílico, donde la fase acuosa fue descartada y a la orgánica se le añadió sulfato de magnesio anhidro, dejando en agitación durante 30 min; esta solución se destiló a una temperatura de 218 ºC.
Reacciones de Hidroformilación
Reactivos y Equipos
La manipulación de los reactivos y las reacciones de síntesis y de catálisis en fase homogénea y en medio bifásico acuoso se llevaron a cabo bajo atmósfera inerte utilizando líneas de vacío y técnicas de Schlenk.
Los diferentes gases [nitrógeno, monóxido de carbono, aire sintético, hidrógeno y gas de síntesis (Praxair Venezuela, S.A)] se utilizaron directamente sin purificación previa. Los solventes [tolueno (E M Science); metanol, (Riedel-de Haën), entre otros] fueron de grado analítico. La trifenilfosfina, la 1,2-bis(difenilfosfino)etano (dppe), la 1,3-bis(difenilfosfino)propano (dppp), la 1,4-bis(difenilfosfino)butano (dppb) y la 1,1,1-tris(difenilfosfinometil)etano (trifos) [Aldrich], el cloruro de paladio y el cloruro de rodio [Strem Chemicals], y otros reactivos fueron de grado analítico y se utilizaron sin purificación previa.
Las reacciones catalíticas se realizaron en un reactor de acero Parr Instruments de 125 mL, modelo 4561, el cual consta de un puerto para la extracción de muestras y de una consola donde se pueden medir digitalmente la presión, la temperatura y la velocidad de agitación de la mezcla de reacción. La composición de las mezclas se analizaron utilizando un cromatógrafo de gases marca VARIAN Serie 3300, acoplado a un detector de ionización a la llama (FID) y una columna de acero inoxidable (20% SP-2100, 0.1% carbowax, 100/120 supelcoport), utilizando nitrógeno como fase móvil [Condiciones: Tiny = 220 °C, Tdet = 250 °C; Programa: To = 140°C (2 min), 25 °C/min, Tf = 200 °C (15 min)]. La cuantificación de los resultados se realizó mediante un computador conectado al cromatógrafo a través de una interface Measurement Computing, utilizando el Software Cromat 1.2. Adicionalmente, los productos de estas reacciones se caracterizaron en un cromatógrafo de gases HEWLETT PACKARD 5890 SERIE II PLUS con detector cuadrupolar de masa (impacto electrónico) y una columna ULTRA HP-2 (5% de fenilmetilsilicona) de 25 m, utilizando helio como gas de arrastre; la cuantificación se llevó a cabo en un computador HP VECTRA XM SERIE III acoplado al espectrómetro de masa.
Síntesis de los Precursores Catalíticos
El complejo Rh(acac)(CO)2 se sintetizó de acuerdo al método reportado en la literatura. [25] Los precatalizadores de rodio que se utilizaron en las reacciones de hidroformilación catalítica de oleato de metilo se formaron in situ en el medio de reacción por reacción del complejo dicarbonilico con los equivalentes necesarios de la fosfina correspondiente.
Síntesis de Esteres Metílicos de Ácidos Grasos
El sustrato oleato de metilo se sintetizó por esterificación del ácido oleico con metanol en presencia de ácido sulfúrico como catalizador. En un balón de 250 mL se colocaron el ácido oleico (50 mL, 0,16 moles) y un exceso de metanol (12,7 ml, 0,31 moles), en presencia de ácido sulfúrico como catalizador (1,54 mL, 0,028 moles). La solución se colocó bajo reflujo constante con ayuda de una manta de calentamiento a una temperatura aproximada de 100 ºC, para así de esta forma eliminar la mayor cantidad de agua que se forma en la reacción. El pH de la mezcla (pH≈ 9) se reguló agregando bicarbonato de sodio. El líquido se separó por decantación y se lavó con éter dietílico, donde la fase acuosa fue descartada y a la orgánica se le añadió sulfato de magnesio anhidro, dejando en agitación durante 30 min; esta solución se destiló a una temperatura de 218 ºC.
Reacciones de Hidroformilación
Las reacciones de hidroformilación en fase homogénea se llevaron a cabo en un vaso de vidrio PYREX dentro de un autoclave de acero, donde se colocaron el sistema catalítico (sal o complejo metálico y la fosfina), el sustrato olefinico (oleato de metilo o el aceite vegetal) y el solvente tolueno (volumen total de reacción 30 mL). El autoclave se desoxigenó mediante tres ciclos de carga y descarga con gas inerte y se comenzó a calentar hasta alcanzar la temperatura de trabajo (100 °C), momento en el cual se cargará con la presión determinada de gas de síntesis (tiempo cero de reacción). Se tomaron muestras de la mezcla de reacción periódicamente y se analizaron por cromatografía de gases.
RESULTADOS Y DISCUSIÓN
La carbonilación de ésteres de ácidos grasos, en especial la hidroformilación, se ha convertido en un área muy innovadora para la industria de la química fina y la síntesis orgánica. Sin embargo, existen muy pocos ejemplos de estudios sobre el uso de catalizadores de hidroformilación para este tipo de sustratos. En las reacciones de hidroformilación se han usado principalmente catalizadores de cobalto, rodio y rutenio, pero los complejos de rodio han sido los precatalizadores más eficientes, ya que bajo condiciones suaves de reacción se han conseguido las mayores actividades y selectividades. [26] En algunas investigaciones se ha determinado que para las reacciones de hidroformilación los precatalizadores más activos son aquellos basados en sistemas de rodio que contienen trifenilfosfina, tales como el complejo RhH(CO)(PPh3)3 o el sistema formado in situ por reacción de Rh(acac)(CO)2, con tres equivalentes de trifenilfosfina (PPh3). En el presente trabajo se llevó a cabo un estudio de la hidroformilación de oleato de metilo (OM ) catalizada por sistemas catalíticos de rodio, conteniendo fosfinas mono-, bi- y tridentadas. La selección de los sistemas catalíticos se basó en varios hechos fundamentales:
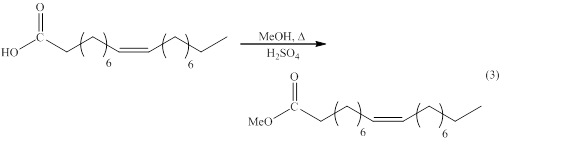
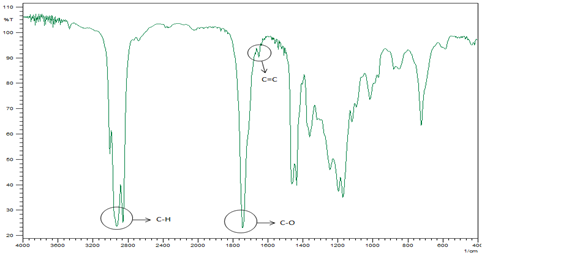
Figura 4. Espectro infrarrojo del oleato de metilo.
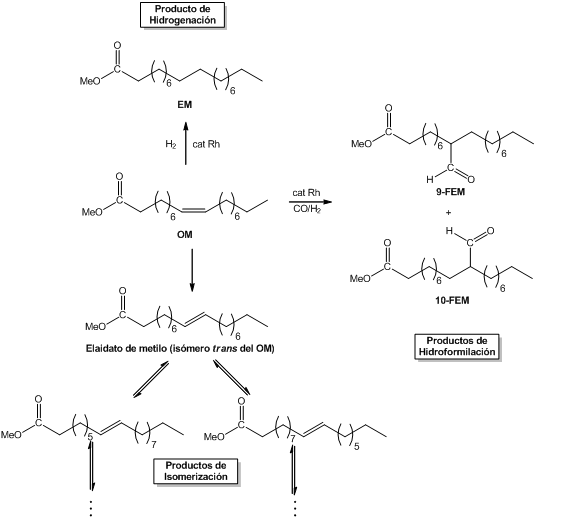
Figura 5. Productos posibles de la reacción de hidroformilación del oleato de metilo.
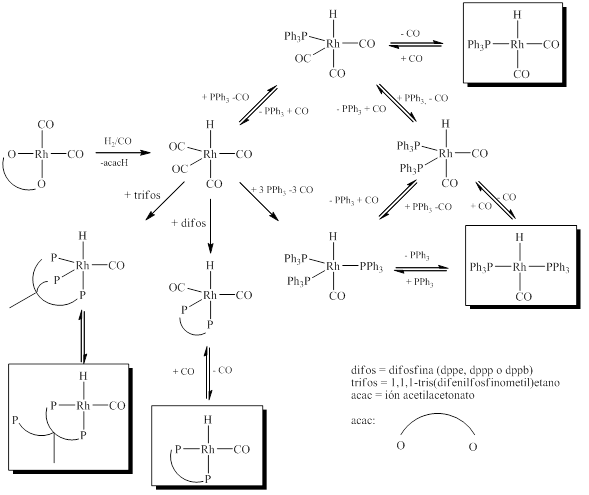
Figura 6. Especies organometálicas que se forman en las reacciones de hidroformilación con sistemas de Rh con fosfinas mono, bi- y tridentadas.
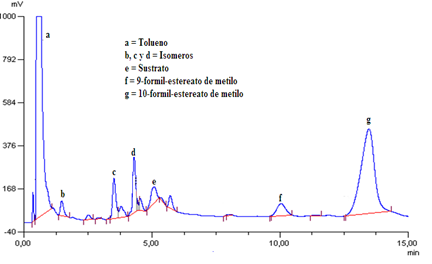
Figura 7. Cromatograma característico de la reacción de hidroformilación de oleato de metilo catalizada por sistemas de rodio.
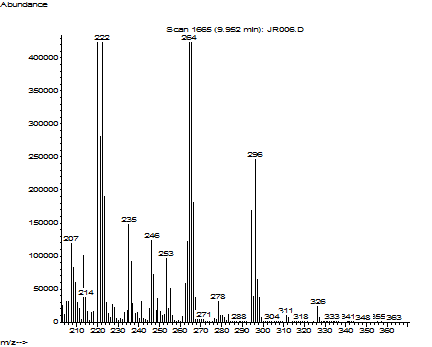
Figura 8. Espectro de masas del producto mayoritario de la hidroformilación del oleato de metilo: 9-formilestearato de metilo (9-FEM).
>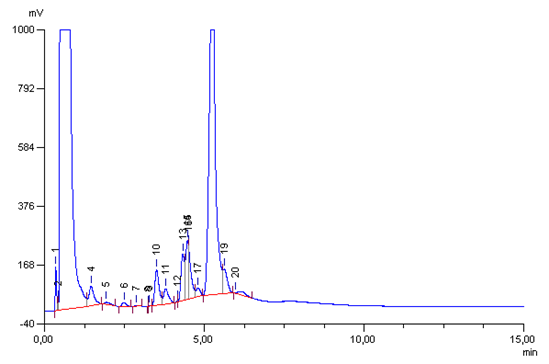
Figura 9. Cromatograma característico de la reacción de isomerización de oleato de metilo catalizada por el sistema Rh/3PPh3.
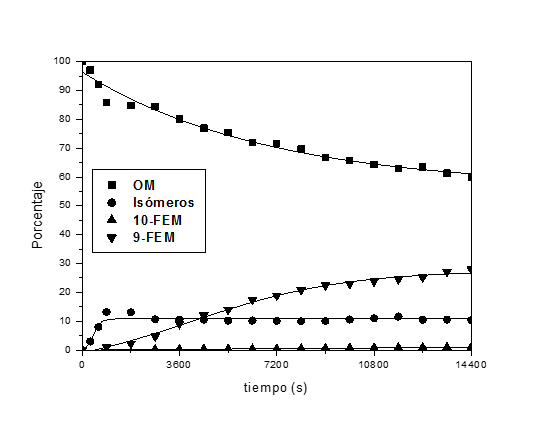
Figura 10. Perfil de reacción de la hidroformilación del oleato de metilo catalizada por el sistema Rh/3PPh3.
Condiciones: [Rh] = 1,25 mM, [OM] = 0,125 M, T = 100ºC, t = 4h, solvente: tolueno (Vtotal = 40 mL)
Los complejos de metales del grupo 9, principalmente rodio, son catalizadores muy activos para reacciones de hidroformilación de olefinas.
La presencia de fosfinas como ligandos espectadores debe, por un lado estabilizar ligeramente el precursor catalítico y por el otro producir a través de sus efectos electrónicos y estéricos una mayor actividad catalítica y selectividad. En las reacción de hidroformilación, el exceso de ligandos fosfina monodentadas o la presencia de fosfinas polidentadas permite formar especies catalíticas que poseen dos o más átomos de fósforo coordinados, las cuales se ha demostrado producen mayor actividad catalítica y selectividad, que las que contienen un solo átomo de fósforo coordinado.
Para la hidroformilación de olefinas, los sistemas de rodio muestran una tendencia a formar con facilidad complejos organometálicos carbonílicos, uno de los ligandos participativos de la reacción de hidroformilación de olefinas.
Para las reacciones de hidroformilación en medio bifásico-acuoso, el uso de fosfinas sulfonadas permite formar una especie organometálica soluble en agua, mientras que los sustratos olefínicos (ésteres de ácidos grasos) estarían en la fase orgánica, lo cual permite una separación fácil del catalizador (generalmente por decantación).
Hidroformilación Homogénea de Oleato de Metilo Catalizada por Sistemas Rh/fosfina
El sustrato que se utilizó (oleato de metilo) se sintetizó a través de la esterificación del ácido oleico con metanol en presencia de ácido sulfúrico como catalizador (ec. 3).

En esta esterificación se obtuvo un producto incoloro con un olor característico a aceite vegetal, con un rendimiento de 90%; la pureza de este compuesto se verificó empleando cromatografía gas-líquido y espectroscopía IR. En el espectro IR del oleato de metilo (Figura 4), se observaron las señales características del estiramiento C-H alifático a 2908 y 2864 cm-1, así como las del estiramiento de los dobles enlaces C=O y C=C a 1745 y 1560 cm-1; estas señales coinciden con las reportadas en la literatura. [27]

En la Figura 5 se muestran los productos de hidroformilación de este sustrato, el 9- y el 10-formilestearato (FEM); sin embargo, bajo las condiciones de reacción es posible la formación de algunos sub-productos, tales como el compuesto saturado originado por la hidrogenación del doble enlace C=C, el estearato de metilo (EM) o compuestos insaturados producto de la isomerización del sustrato, isomerización cis-trans a eliadato de metilo o por migración de doble enlace, [28] lo cual a su vez pueden conducir a la formación de otros FEM por su consecuente hidroformilación.

Los complejos de rodio que se utilizaron como precatalizadores en las reacciones de hidroformilación de oleato de metilo (OM) se formaron in situ por adición de uno o tres equivalentes de trifenilfosfina (Rh/PPh3 y Rh/3PPh3, respectivamente), de un equivalente de fosfinas bidentada (Rh/difos), tales como la 1,2-bis(difenilfosfino)etano, la 1,3-bis(difenilfosfino)propano (dppp), la 1,4-bis(difenilfosfino)butano (dppb), o de un equivalente de la fosfina tridentada 1,1,1-tris(difenilfosfinometil)etano (Rh/trifos) al complejo Rh(acac)(CO)2. Se ha reportado que bajo las condiciones de hidroformilación estos sistemas forman complejos hidruro-carbonilo de rodio (I) de estructura bipirámide trigonal (bpt), que por disociación de un ligando generan las especies catalíticamente activas (ECA) correspondientes de estructura plano cuadrada, tal como se muestra en la Figura 6. Cuando se adiciona un equivalente de trifenilfosfina, la ECA que se genera es RhH(CO)2(PPh3) mientras que usando tres equivalentes de trifenilfosfina se favorece la especie con dos trifenilfosfina, RhH(CO)(PPh3)2. Para los sistemas con fosfinas bi- y tridentadas se favorecen especies hidruro-carbonilo enlazados de modo η2, es decir con dos átomos de fósforo coordinados. [29, 30]

Los precursores Rh/fosfina mostraron ser catalíticamente activos para la hidroformilación homogénea de OM bajo condiciones moderadas de reacción. Se observó, además de la formación de algunos isómeros, dos productos de hidroformilación.
En el cromatograma correspondiente a la hidroformilación del oleato de metilo (Figura 7), se puede observar la presencia del solvente tolueno (tr = 0,5 min) y del sustrato (tr = 5,1 min), los cuales se identificaron por comparación con los tiempos de retención (tr) de muestras puras. Adicionalmente, se observaron al menos ocho compuestos con tr entre 1,5 y 6,0 min, muy cercanos al tr del sustrato y dos picos a tr de 10,0 y 13,1 min. El pico que aparece a un tiempo de retención de 13,1 min corresponde a uno de los productos de hidroformilación del oleato de metilo, el 9-formilestearato de metilo (9-FEM), como pudo ser comprobado por GC-MS.
El espectro de masas del producto mayoritario (Figura 8) muestra el pico del ion molecular a M+ 326 u.m.a, el cual corresponde a la masa molecular de dicho aldehído. El siguiente pico se observa a una relación m/z de 296 u.m.a asignable a la pérdida de 30 u.m.a correspondiente a la generación de formaldehido. Además, se observaron dos picos de mayor intensidad (pico base) a 264 y 222 u.m.a, respectivamente; el primero correspondiente a la disminución de 32 unidades del fragmento de 296 u.m.a. (pérdida de metanol) y el segundo corresponde a la pérdida de 74 unidades del fragmento de 296 u.m.a. por la formación del enolato MeOC(OH)=CH2 a través del rearreglo de McLafferty. Finalmente el pico de 214 u.m.a. corresponde al fragmento M+1 producto de la pérdida de 113 unidades del pico de ión molecular, lo que establece que el grupo formilo se encuentra en posición 9. Sobre la base de estos resultados se puede inferir que el producto mayoritario es el 9-formilestearato de metilo (9-FEM), mientras que el producto minoritario podría ser el 10-FEM. En ninguna de las reacciones se observó la formación del producto de hidrogenación, el estearato de metilo (EM).
El compuesto con tr de 10,0 min no pudo ser caracterizado, pero por analogía con otros trabajos de hidroformilación de OM con sistemas de Rh, pudiera asignarse al otro producto de hidroformilación del OM, el 10-FEM.


Las señales que aparecen en el cromatograma correspondiente a la reacción de hidroformilación de OM aparecen a tiempos de retención entre 1,25 y 6,0 min corresponden a subproductos de isomerización. Esto se pudo corroborar haciendo la reacción catalítica en ausencia de gas de síntesis (CO e H2).En esta reacción se pudo observar un 22% de productos de isomerización total (al menos diez isómeros) en un tiempo de 4h como se pude verificar a través del cromatograma de esta reacción (Figura 9). El producto de hidrogenación del OM (estearato de metilo, EM) y los productos de hidrogenación de los aldehídos grasos derivados del OM no fueron observados en las reacciones catalíticas de hidroformilación de OM con sistemas Rh conteniendo ligandos fosfinas.

Un perfil de la hidroformilación de OM con el sistema de Rh/3PPh3, el sistema más activo, se muestra en la Figura 10. Como se puede observar en los primeros 15 min (900 s) se observa únicamente la formación de isómeros (13%) y a partir de ese momento se comienza a formar el 9-FEM, incrementándose linealmente en las primeras 2 h (7200 s), alcanzando un 28% en el transcurso de 4 h (14.400 s); el 10-FEM se obtiene solamente en un 1% mientras que los isómeros se mantienen en un porcentaje alrededor del 10% durante toda la reacción.
Si se toman en cuenta la porción lineal de la gráfica de concentración molar de aldehídos en función del tiempo en segundos se puede determinar la velocidad inicial de la reacción.

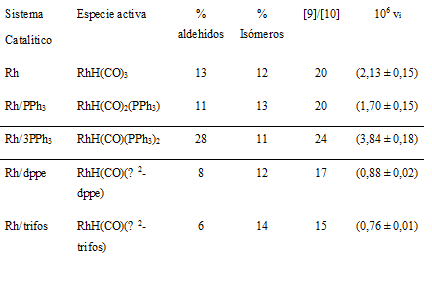
En la Tabla 1 se muestran los resultados de actividad catalítica en porcentaje de conversión (4 h) y en velocidad inicial (vi) para los sistemas Rh/fosfina; se evaluó la actividad de sistema de rodio no modificado con fosfina (Rh) para efectos de comparación. Como se puede observar, el orden de actividad catalítica fue Rh/3PPh3 > Rh > Rh/PPh3 > Rh/dppe > Rh/trifos. Este es el primer estudio del uso de sistemas de rodio con fosfinas bi- y tridentadas reportado en la literatura. Los sistemas de rodio/fosfinas requieren de un periodo de inducción para la formación de las especies activas menor a 10 min para el sistema no modificado de rodio, de alrededor de 10 min para los sistemas con trifenilfosfina y mayor de 15 min para los sistemas con fosfinas bi- y tridentadas (dppe y trifos). Los porcentajes de isomerización oscilan entre 11 y 14%, mientras que las relaciones entre el producto 9-FEM y 10-FEM (relación [9]/[10]) es 20 y 24 para los sistemas con trifenilfosfina (1 y 3 equivalentes, respectivamente) y menores para las fosfinas polidentadas (17 y 15 para el sistema con dppe y trifos, respectivamente). La variación de los equivalentes de PPh3 no afecta significativamente la actividad hacia los productos de hidroformilación ni de los sub-productos.
Tabla 1. Actividades catalíticas y selectividades para la hidroformilación de oleato de metilo con los sistemas Rh/fosfina, bajo condiciones moderadas de presión de gas de síntesis (15 atm).

Hidroformilación homogénea de mezclas de AV catalizada por los sistemas de rodio y cobalto conteniendo trifenilfosfina
Los aceites vegetales destinados al consumo humano han sido usados para la producción comercial de biodiésel. La utilización de estos aceites producidos a partir de materias primas abundantes está ampliamente documentada en países donde se estudia a profundidad su viabilidad como fuentes de biodiésel. [17] La Moringa oleifera, por ser una planta de crecimiento rápido, resistente a la sequía y con un alto rendimiento de aceite, es una excelente opción para la producción sostenible de biodiésel en países con tierras áridas. Este aceite tiene un alto contenido de ácido oleico (ca.> 70%) con ácidos grasos saturados que comprenden la mayor parte del perfil de ácidos grasos restante. [31] La borra de café es otro de los materiales que presentan niveles altos de grasas, siendo el principal componente el ácido linoleico (48%). [19]
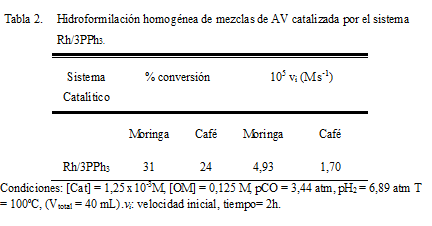
Sobre la base de estos antecedentes, en el presente trabajo se llevó a cabo la hidroformilación del aceite de moringa y de la grasa de la borra del café (Tabla 2) utilizando sistemas de Rh con trifenilfosfina.

El precursor Rh/3PPh3 mostró ser catalíticamente activo para la hidroformilación homogénea de AV bajo condiciones moderadas de reacción. La actividad del sistema de rodio fue mayor para la hidroformilación del AV derivado de la moringa que la hidroformilación del oleato de metilo puro.
Finalmente para la grasa derivada de la borra de café, el sistema de rodio resultó ser activo para la hidroformilación de esta grasa, la cual es rica en ácido linoleico, formando en este caso un derivado de tipo diformilestereato. Estos derivados diformilo son importante debido a su aplicación en la producción de poliuretanos. Así mismo puede ser utilizado como combustible ya que se conoce que anteriormente se utilizaban estos aceites vegetales puros como biocombustibles pero debido a su alta masa molar y a su viscosidad alta se le practica una trans-esterificación rompiendo el esqueleto glicerina y los éster obtenidos utilizarlos como biodiesel, en tal sentido, en este trabajo (que aún está en crecimiento) se está buscando mejorar esas propiedades, además de tratar de minimizar los gastos que tienen las industrias (reactivos, entre otros) así como también, el impacto ambiental que estas generan.
En mi siguiente post les estaré hablando un poco sobre la catálisis bifásica. Espero les gustara este post. Saludos amigos
REFERENCIAS
20. Sanchez, I.; Huertas, K., 2012, “Obtención y caracterización de biodiesel a partir de aceite de semillas de ricinuscommunis. (higuerilla) modificadas géneticamente y cultivadas en el eje cafetero”, Tesis de pregrado. Escuela de Química, Facultad de Tecnología, Universidad
21. Anwar, F.; Bhanger, M., 2003, “Analytical Characterization of Moringa oleifera Seed Oil Grown in Temperate Regions of Pakistan”, Journal of Agricultural and Food Chemistry, 51, 6558-6563
22. Fernandes, D.; Sousa, R.; Oliveira, A.; Morais, S.; Richter,E.; Muñoz, R., 2015, “Moringa oleifera: A potential source for production of biodiesel and antioxidant additives”, Fuel, 146, 75–80
23. Frankel, E.N.; Thomas, F.L., 1972, “Selective Hydroformylation of Polyunsaturated Fats with a Rhodium–Triphenylphosphine Catalyst”, J. Am. Oil Chem. Soc. 49, 10–14.
24. Frankel, E.N.; Thomas, F.L., 1972, “Selective Hydroformylation of Polyunsaturated Fats with a Rhodium–Triphenylphosphine Catalyst”, J. Am. Oil Chem. Soc. 49, 10–14.
25. Varshavskii, Y.S.; Cherkasova, T.G., 1967, “A simple method for preparing acetyl-acetonatodicarbonylrhodium(I)”, Russ. J. Inorg. Chem. Engl. Transl., 12, 899-900.
26. Ciprés, I.; Kalck, P.; Park, D.; Serein-Sipirau F., 1991, “Carbon monoxide as a building block for organic synthesis. Part III. Selective hydrocarbonylation of monoterpenes to give potentially biologically active aldehydes”, J. Mol. Catal., 66, 399-407.
27. SDBS, 1997, Base de datos espectrales para compuestos organicos, Japón, Pag 2, Consultada el 23/01/2012
28. Andielkovic, D.D.; Min, B.; Ahn, D.; Larock R.C., 2006, “Elucidation of structural isomers from the homogeneous rhodium-catalyzed isomerization of vegetable oils”, J. Agric. Food Chem., 54, 25, 9535-9543.
29. Joó, F., 2001, Aqueous organometallic catalysis, in catalysis by metal complexes (Eds. James B., van Leeuwen P.W.N.M.), Kluwer Academic Publishers, Dordrecht (The Netherlands), 1-9.
30. Herrmann, W.A.; Kohlpaintner, C.W., 1993, “Water-Soluble Ligands, Metal Complexes, and Catalysts: Synergism of Homogeneous and Heterogeneous Catalysis”, Angew. Chem. Int. Engl., 32, 11, 1524-1544.
31. Rashid, U.; Anwar F.; Moser, B.; Knothe, G., 2008, “Moringa oleifera oil: A possible source of biodiesel”, Bioresource Technology, 99, 8175–8179.
Hola Jairo. Saludos. Resulta interesante tu post. Sin embargo te recomiendo no sean tan largos para que resulte mas agradable la lectura. Tambien te recomiendo pases a leer algunas de las sugerencias del tag #stem-espanol para que te sean útiles en tu próxima publicación. te apoyo con mi voto
gracias amiga tomare en cuenta tu recomendación para mis siguientes post, saludos